產(chǎn)品列表
聯(lián)系我們
021-35322621
- 地址:
- 上海市虹口區(qū)公平路761號4樓A座
- 郵箱:
- tonylee@huiyuanlog.com
- Q Q:
- 496698609
- 電話:
- 86-021-35322621
中藥材進口清關(guān)
中藥材進口清關(guān)
添加時間:2017-12-12


進口藥材流程
一、申請和審批
1、首次進口藥材:
首先確定進口藥材紅花的使用或經(jīng)營公司。
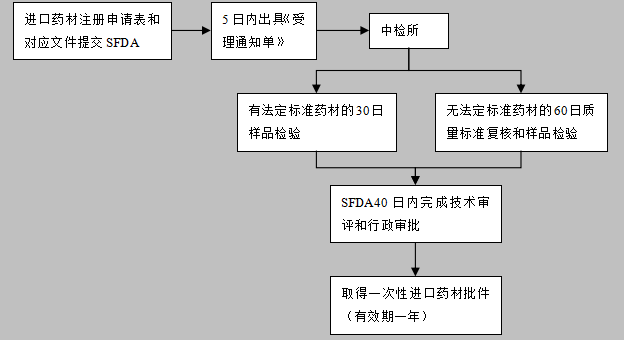
注: SFDA為:國家食品藥品監(jiān)督管理總局
2、非首次進口藥材
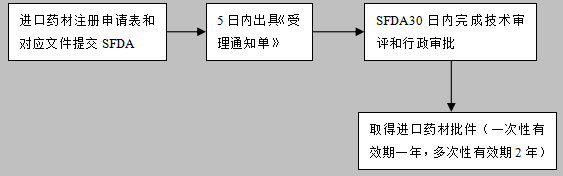
二、邊境或口岸藥監(jiān)局登記備案

三、口岸檢驗和監(jiān)督管理
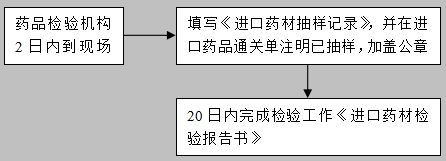
四、所需提交資料
1、首次進口藥材上報SFDA:
申請人需報送下列資料一式兩份,分別提交國家食品藥品監(jiān)督管理局和中國藥品生物制品檢定所。
(一)《進口藥材申請表》。
(二)申請人《藥品經(jīng)營許可證》或《藥品生產(chǎn)許可證》、《營業(yè)執(zhí)照》(復(fù)印件)。
(三)供貨方合法登記證明文件(如《營業(yè)執(zhí)照》等)(復(fù)印件)。
(四)購貨合同(復(fù)印件)。
(五)藥材質(zhì)量標準及其來源。
(六)藥材基源研究證明資料(研究證明資料應(yīng)由中國境內(nèi)具有動、植物基源鑒定資質(zhì)的機構(gòu)提供)。
其中,如進口藥材的質(zhì)量標準來源于省、自治區(qū)、直轄市藥材標準,申請人除報送上述資料外,還應(yīng)根據(jù)具體情況,對該標準作相應(yīng)的提高工作,并報送有關(guān)研究資料;如進口藥材無法定標準,申請人除報送上述資料外,還應(yīng)報送下述資料:
1、藥材生態(tài)環(huán)境、生長特征、形態(tài)描述、栽培或者培植(培育)技術(shù)、產(chǎn)地加工等。
2、藥材質(zhì)量標準起草說明。
3、藥理毒理研究資料綜述。
4、主要藥效學(xué)試驗資料及文獻資料。
5、一般藥理研究的試驗資料及文獻資料。
6、急性毒性試驗資料及文獻資料。
7、我國批準的中成藥處方中含有該藥材的證明資料。
2、非首次進口藥材上報SFDA
申請人需報送下述資料一式一份。
(一)《進口藥材申請表》。
(二)申請人《藥品經(jīng)營許可證》或者《藥品生產(chǎn)許可證》、《營業(yè)執(zhí)照》(復(fù)印件)。
(三)供貨方合法登記證明文件(如《營業(yè)執(zhí)照》等)(復(fù)印件)。
(四)購貨合同(復(fù)印件)。
(五)藥材質(zhì)量標準及其來源。
3、登記備案上報口岸藥監(jiān)局
申請人需報送下列資料一式兩份。
一、《進口藥材批件》復(fù)印件(和《進口藥材補充申請批件》復(fù)印件)。
二、申請人的《藥品經(jīng)營許可證》或者《藥品生產(chǎn)許可證》復(fù)印件。
三、原產(chǎn)地證明復(fù)印件。
四、購貨合同復(fù)印件。
五、裝箱單、提運單和貨運發(fā)票復(fù)印件。
六、經(jīng)其他國家或者地區(qū)轉(zhuǎn)口的進口藥材,應(yīng)當同時提交從原產(chǎn)地到各轉(zhuǎn)口地的全部購貨合同、裝箱單、提運單和貨運發(fā)票。
七、涉及瀕危物種的藥材,應(yīng)當提供進出口雙方國家瀕危物種進出口管理機構(gòu)證明文件復(fù)印件。上述各類復(fù)印件應(yīng)當加蓋申請人公章。
下一篇:沒有了
上一篇:沒有了


